INTRODUÇÃO
Em exames de endoscopia digestiva alta de rotina, o achado de lesão subepitelial em esôfago é ocasional, porém presente com certa frequência.
Geralmente, o paciente se apresenta assintomático quanto à lesão encontrada, e o exame endoscópico foi indicado por outras causas, tais como dispepsia, suspeita de refluxo gastroesofágico, empachamento, etc (Figura 1).
Apesar da sintomatologia não estar relacionada à lesão subepitelial encontrada, seu esclarecimento diagnóstico nos direciona à investigação mais específica por meio de outros métodos de imagem, como a tomografia computadorizada, a ressonância magnética nuclear e a ecoendoscopia.
Nas lesões subepiteliais, as biópsias da mucosa não esclarecem o seu diagnóstico, justamente por estarem recobertas por mucosa íntegra e não serem representativas da lesão subepitelial.
Porém, quando encontramos uma solução de continuidade da lesão subepitelial com a mucosa (por exemplo, em lesões com ulcerações ou erosões na mucosa que a recobre), as amostras teciduais nas áreas ulceradas ou erodidas, por meio de biópsias endoluminais (pinças tipo fórceps), merecem ser investidas para o diagnóstico histológico.
São várias as hipóteses diagnósticas das lesões subepiteliais em esôfago:
- Cisto de retenção;
- Lipoma submucoso;
- Schwannoma;
- Hemangioma;
- Leiomioma;
- GIST;
- Duplicação cística.
Dentre as possibilidades diagnósticas, a duplicação cística de esôfago deve ser considerada.
DUPLICAÇÃO CÍSTICA ESOFÁGICA
A duplicação cística é decorrente de alterações da formação do tubo digestório. Na fase embrionária, a endoderme se divide em 3 segmentos distintos:
- intestino primitivo cefálico (foregut);
- intestino primitivo médio (midgut);
- intestino primitivo caudal (hindgut).
Para a formação do segmento proximal do tubo digestivo (3ª a 8ª semana de gestação) [1], o intestino primitivo cefálico (foregut), que se constitui como um único tubo, divide-se em 2 tubos paralelos e origina 2 segmentos tubulares:
- Segmento anterior: que forma a traqueia e seus ramos segmentares;
- Segmento posterior: que origina o todo o esôfago.
Uma grande falha na junção da endoderme possibilita uma fusão anômala e, consequentemente, formam as atresias de esôfago e de traqueia (total ou parcial) associadas ou não à fistula esofagotraqueal.
Esporadicamente, pode haver uma junção irregular dos bordos de fusão, de maneira a resultar em um recesso intramural no esôfago, ou mesmo um recesso para-esofágico (extramural), o qual origina a duplicação cística do esôfago (Figura 2).

Figura 1a: intestino primitivo cefálico com formação de traqueia e esôfago.
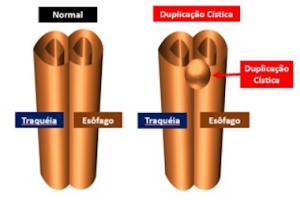
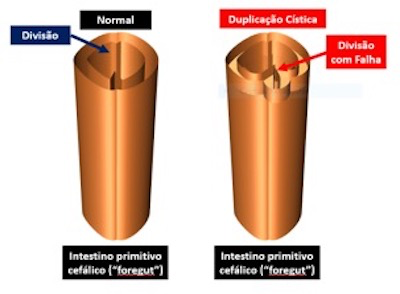
Figura 2: a) Intestino primitivo cefálico com formação de traqueia e esôfago. b) Intestino primitivo cefálico com falha e formação de duplicação cística.
Histologicamente, o interior da duplicação cística de esôfago é revestido por epitélio escamoso ou entérico, os quais secretam secreção seromucosa. Externamente, é formada por dupla camada de musculatura lisa e, raramente, pode apresentar uma comunicação nítida com a luz esofágica.
Quanto à localização esofágica, a maior parte das duplicações císticas situam-se na região posterolateral direita do mediastino inferior e com maior predominância no terço distal (2/3) comparado ao terço proximal e médio (1/3) [2].
Por ser uma malformação congênita, o diagnóstico é mais frequente em crianças (80%) [3], as quais apresentam sintomas. No adulto, a sintomatologia geralmente é ausente, e, quando se apresenta algum sintoma (< 7%), está relacionado ao efeito compressivo da lesão em órgãos adjacentes [2]. Assim, a sintomatologia pode variar em função da localização da duplicação cística no esôfago (tabela 1).
| Localização em esôfago | Sintoma relacionado |
| 1/3 proximal | estridor, tosse |
| 1/3 médio | dor torácica, disfagia |
| 1/3 distal | disfagia, epigastralgia, vômitos, arritmia cardíaca [4] |
INVESTIGAÇÃO DIAGNÓSTICA
Tomografia Computadorizada (CT): identifica-se uma imagem de massa homogênea, com íntimo contato com o esôfago, arredondada ou ovalada, bem delimitada, de contornos regulares, associada à densidade de fluido no seu interior e que não se altera à injeção de contraste.
Ressonância Magnética Nuclear (RMN): demonstra formação cística, localizada junto à parede esofágica, com hipossinal em T1, hipersinal em T2 e sem aspecto sólido em T1 com contraste.
Ecoendoscopia:
É indicada [5]:
- Quando CT ou RMN não definem diagnóstico;
- Em lesões suspeitas de malignidade;
- Em formações atípicas.
A imagem ecográfica típica de duplicação cística de esôfago tem ecotextura anecoica ou hipoecoica, homogênea, alongada ou ovalada, de contornos regulares, limites precisos, com reforço hiperecoico no seu limite posterior. Situa-se inserida em camada submucosa, muscular própria ou até mesmo subserosa, com 3 a 5 camadas na parede [3] (Figura 3). Por vezes, podem ser múltiplas formações císticas intramurais com lobulações, e até mesmo, com septações em sua parede [6] (Figura 4). O conteúdo intracístico também pode ser heterogêneo, com imagens de debris ou pontos puntiformes de permeio (Figura 5).
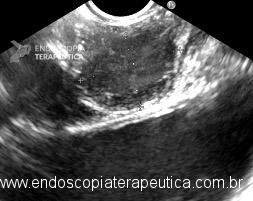
Figura 3: ecoendoscopia setorial com imagem hipoecoica inserida em camada submucosa e muscular própria de esôfago distal.

Figura 4: ecoendoscopia radial com imagem anecoica inserida em camada submucosa e muscular própria de esôfago com septos finos.
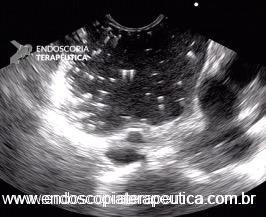
Figura 5: ecoendoscopia setorial com imagem hipoecoica inserida em camada submucosa e muscular própria de esôfago distal com pontos hiperecoicos de permeio.
A princípio, a diferenciação quanto à natureza sólida ou cística da imagem pode ser definida pela ecoendoscopia. Porém mesmo ecoendoscopistas experientes podem ter dúvidas, uma vez que a secreção espessa da duplicação cística (muco) pode mimetizar uma imagem sólida ecográfica.
Nessas situações, a punção ecoguiada se faz necessária para possibilitar o diagnóstico diferencial entre duplicação cística de esôfago, leiomioma, GIST ou mesmo um conglomerado linfonodal paraesofágico. A amostra da punção ecoguiada pode revelar material mucoide com células epiteliais, semelhantes ao epitélio esofágico ou entérico. A grande preocupação em relação à punção ecoguiada é a infecção. Com taxas de 14% [4] [8], a infecção intracística pós-punção ecoguiada se demonstrou com morbidade e mortalidade temerárias pela potencial evolução para mediastinite, mesmo com uso de antibióticos em doses terapêuticas. Assim, há uma tendência dos ecoendoscopistas em reservar a punção ecoguiada somente em casos extremamente necessários [9].
O tratamento da duplicação cística de esôfago é indicado em pacientes sintomáticos. A remoção ou a enucleação cirúrgica estão sendo os tratamentos de eleição.
Nos pacientes assintomáticos, o tratamento conservador é predominante frente aos riscos inerentes da cirurgia esofágica (fístula, refluxo gastroesofágico) e mortalidade cirúrgica de 1% [10]. Outros advogam que a baixa taxa anual de crescimento da duplicação cística de esôfago não justifica a morbimortalidade da cirurgia [11]. Há relatos de indicações cirúrgicas em pacientes assintomáticos, justificadas pelo risco de ulceração ou perfuração da duplicação cística de esôfago, com sucesso no seguimento [12].
Saiba mais:
Guideline comentado da ASGE sobre lesões subepiteliais TGI
Tumor de células granulares no esôfago
QUIZ! – Lesão subepitelial de esôfago
Como citar este artigo:
Matuguma, SE. Duplicação cística de esôfago. Endoscopia Terapêutica; 2021. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/duplicacao-cistica-de-esofago
Referências
- Nobuhara KK, Gorski YC, La Quaglia MP, Shamberger RC. Bronchogenic cysts and esophageal duplications: common origins and treatment. J Pediatr Surg [Internet]. 1997 Oct;32(10):1408–13. Available from: http://www.ncbi.nlm.nih.gov/pubmed/9349757
- Pisello F, Geraci G, Arnone E, Sciutto A, Modica G, Sciumè C. Acute onset of esophageal duplication cyst in adult. Case report. G Chir [Internet]. 30(1–2):17–20. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19272226
- Whitaker JA, Deffenbaugh LD, Cooke AR. Esophageal duplication cyst. Case report. Am J Gastroenterol [Internet]. 1980 Apr;73(4):329–32. Available from: http://www.ncbi.nlm.nih.gov/pubmed/7416128
- Bowton DL, Katz PO. Esophageal cyst as a cause of chronic cough. Chest [Internet]. 1984 Jul;86(1):150–2. Available from: http://www.ncbi.nlm.nih.gov/pubmed/6734280
- Adler D, Liu R. Duplication cysts: Diagnosis, management, and the role of endoscopic ultrasound. Endosc Ultrasound [Internet]. 2014;3(3):152. Available from: http://www.eusjournal.com/text.asp?2014/3/3/152/138783
- Bhatia V, Tajika M, Rastogi A. Upper gastrointestinal submucosal lesions–clinical and endosonographic evaluation and management. Trop Gastroenterol [Internet]. 31(1):5–29. Available from: http://www.ncbi.nlm.nih.gov/pubmed/20860221
- Wildi SM, Hoda RS, Fickling W, Schmulewitz N, Varadarajulu S, Roberts SS, et al. Diagnosis of benign cysts of the mediastinum: the role and risks of EUS and FNA. Gastrointest Endosc [Internet]. 2003 Sep;58(3):362–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/14528209
- Cevasco M, Menard MT, Bafford R, McNamee CJ. Acute Infectious Pseudoaneurysm of the Descending Thoracic Aorta and Review of Infectious Aortitis. Vasc Endovascular Surg [Internet]. 2010 Nov 30;44(8):697–700. Available from: http://journals.sagepub.com/doi/10.1177/1538574410376449
- Béchade D, Desramé J, Algayres JP. Gastritis cystica profunda in a patient with no history of gastric surgery. Endoscopy [Internet]. 2007 Dec;39(S 1):E80–1. Available from: http://www.thieme-connect.de/DOI/DOI?10.1055/s-2006-945070
- Salo JA, Ala-Kulju K V. Congenital esophageal cysts in adults. Ann Thorac Surg [Internet]. 1987 Aug;44(2):135–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/3619537
- Versleijen MW, Drenth JP, Nagengast FM. A Case of Esophageal Duplication Cyst with a 13-year Follow-up Period. Endoscopy [Internet]. 2005 Sep;37(9):870–2. Available from: http://www.thieme-connect.de/DOI/DOI?10.1055/s-2005-870219
- Noguchi T, Hashimoto T, Takeno S, Wada S, Tohara K, Uchida Y. Laparoscopic resection of esophageal duplication cyst in an adult. Dis esophagus Off J Int Soc Dis Esophagus [Internet]. 2003;16(2):148–50. Available from: http://www.ncbi.nlm.nih.gov/pubmed/12823217
Acesse o Endoscopia Terapêutica para tomar contato com mais artigos comentados, assuntos gerais, casos clínicos, quizzes, classificações e mais!
Médico assistente do Serviço de Endoscopia Gastrointestinal do HCFMUSP
Médico colaborador do Serviço de Endoscopia do Instituto de Câncer do Estado de SP (ICESP)
Médico da equipe de Endoscopia do Hospital Alemão Oswaldo Cruz

4 Comentários
Sergio, quais cuidados tomar após eventual punção de um cisto de duplicação? Nos casos em que a imagem é duvidosa, é fácil perceber tratar-se de cisto após a punção? Parabéns pela revisão!
Bruno, você pergunta sobre uma situação comum quando se faz a ecoendoscopia. Muitas vezes, o conteudo mucóide intracístco não nos permite determinar apenas pela imagem sua natureza cística e frequemtemente nos confunde como uma imagem sólida. O sinal de termos puncionado uma lesão cística é quando se identifica, no ato da punção ecoguiada, uma lesão muito amolecida à penetraçào da agulha asdiciada a dificuldade de aspiração de seu conteúdo. Assim, constatada esta situação, imediatamente administra-se o antibiótico intravenoso e decide-se continuar de forma terapêutica por mínimo de 07 dias. Sempre ficar em contato com o paciente para eventual sinal potencial de mediastinite, como febre, queda do estado geral, dor torácica ou hipotensão. Orientar para ptocura médica hospitalr, caso desenvolva infecção.
Parabéns pelo post professor, muito claro e didático. Na maioria dos casos é possível chegar ao diagnóstico ecográfico no entanto, em algumas situações fica a dúvida e ficamos com a situação desconfortável de oferecer a punção ao custo do risco de infeção e sua morbidade considerável.
Qual seria a acurácia dessa punção (para cisto de duplicação) ? Caso paciente/familiares/médico assistente cheguem a conclusão de que o risco é elevado, você faria sugestão de acompanhamento em quanto tempo?
Flavio, obrigado pelo comentário.
A acurácia da punção não está mensurada na literatura. Possivelmente, devido a real dificuldade na punção e a temerosa infecção. Caso
O acompanhamento seja o foco, podese oferecer um novo exame entre 3 a 6 meses. E caso esteja estável, anualmente.