A gastrite atrófica é um achado frequente de exames endoscópicos, sendo um dos fatores de risco para o desenvolvimento de câncer gástrico. Para identificar e estratificar grupos de risco foi criada uma classificação denominada OLGA (Operative Link of Gastritis Assesment), baseada na localização das biópsias e achados histológicos avaliando de forma objetiva o grau de atrofia. A classificação é reprodutível, de fácil execução, permitindo selecionar o grupo de pacientes de maior risco que devem ter seguimento mais rígido, mantendo a custo-efetividade do rastreamento.
Resumidamente, as biópsias devem ser realizadas nos seguintes locais e identificadas em três frascos separados, com ao menos dois fragmentos de cada local:
- Parede anterior e parede posterior de corpo (C1 e C2)
- Incisura angular (A3)
- Pequena e grande curvatura de antro (A1 e A2)
Obs: se quiser uma discussão mais aprofundada a respeito dos locais de biópsia, confira esse outro artigo: onde coletar as biópsias para estadiamento OLGA?
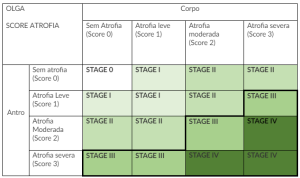
O escore OLGA é classificado de acordo com o resultado destas biópsias, conforme tabela abaixo:
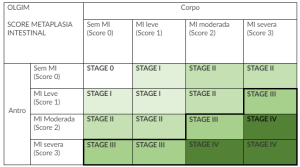
Essa classificação não leva em consideração a avaliação de outro fator de risco relevante caracterizado pela metaplasia intestinal. Para suprir esta deficiência, a classificação de OLGIM foi criada e basicamente reproduz a mesma ideia de avaliar a localização de biópsias com aspectos histológicos, porém voltadas para a metaplasia intestinal.
Os estágios são muito parecidos conforme disposto na tabela abaixo:
É realmente necessário fazer essas biópsias? A avaliação endoscópica não é suficiente??
Diversas publicações mostraram ao longo do tempo que os scores OLGA III/IV possuem maior risco para desenvolvimento de câncer gástrico, sendo relevante realizar seguimento cuidadoso neste subgrupo. Dentre elas destaca-se a publicação da GUT de 2007 envolvendo 448 pacientes estratificados utilizando o sistema OLGA com identificação de aumento gradativo da faixa etária e prevalência de infeção com H. Pylori (HP) nos escores maiores. Além disso, lesões neoplásicas foram identificadas apenas nos estágios OLGA III e IV.
Publicações mais recentes corroboram estes achados como a extensa metanálise envolvendo cerca de 2700 pacientes (8 estudos , dos quais 6 caso-controle) realizada por Yue H et al em 2018. Nessa publicação, foi descrito maior risco de desenvolvimento de câncer gástrico em escores OLGA III e IV (OR 2,64; 95% IC p<0,00001) e OLGIM III e IV (OR 3.99; 95% IC , p< 0,00001), confirmando a importância dos escores descritos nesse post e ressaltando a importância de fazer sim as biópsias.
O que dizem então os guidelines?
ASGE (2021 )
- As biópsias devem ser realizadas em antro, incisura e corpo;
- A presença de metaplasia intestinal implica em diagnóstico de gastrite atrófica;
- Achados endoscópicos típicos: mucosa gástrica pálida, aumento da visualização de vascularização submucosa e perda de pregas gástricas;
- Pacientes com gastrite atrófica e com HP + devem realizar tratamento e confirmar erradicação;
- Rastreamento a cada 3 anos em pacientes com atrofia gástrica avançada (baseado na histologia e extensão de acometimento);
- Na presença de gastrite autoimune, pesquisar vitamina B12, Ferro e anticorpos anticorpos anti-célula parietal e anti-fator intrínseco, doenças tireoideanas. Suspeitar de gastrite autoimune em pacientes com deficiência de B12 e/ou de Ferro;
- Anemia perniciosa é uma manifestação tardia de gastrite autoimune – no diagnóstico realizar biópsias para confirmar predominância de atrofia em corpo e excluir neoplasia e tumores neuroendócrinos;
- Pacientes com gastrite autoimune devem ser rastreados para tumor neuroendócrino tipo 1 e os menores que 1cm devem ser ressecados. Controle endoscópico a cada 1-2 anos.
ESGE (2019 – MAPSII)
- Pacientes com gastrite atrófica ou metaplasia intestinal possuem risco aumentado de adenocarcinoma;
- Endoscopia com equipamentos de alta definição e cromoscopia (CE) são superiores a endoscópios de alta definição com luz convencional
- Cromoscopia pode direcionar as biópsias para áreas mais representativas, com maior risco de malignidade;
- Realizar biópsias em ao menos dois locais (corpo e antro – grande e pequena curvaturas) e enviar em frascos separados;
- Pacientes com atrofia leve a moderada restrita ao antro não possuem evidência para recomendação de rastreamento;
- Pacientes com metaplasia intestinal em uma única região porém com histórico familiar de câncer gástrico, metaplasia incompleta ou gastrite crônica com HP persistente – considerar rastreamento e biópsias guiadas por CE em 3 anos;
- Casos de gastrite atrófica severa devem ser rastreados a cada 3 anos;
- Displasia, sem lesão endoscópica definida devem ser submetidos a endoscopia com CE;
- Lesão endoscópica com displasia de baixo ou alto grau / carcinoma devem ser estadiados e tratados;
- Erradicação de H. pylori traz cicatrização do tecido não atrófico reduzindo o risco de câncer.
Referências:
- Yue, H., Shan, L., & Bin, L. (2018). The significance of OLGA and OLGIM staging systems in the risk assessment of gastric cancer: a systematic review and meta-analysis. In Gastric Cancer (Vol. 21, Issue 4, pp. 579–587).
- Rugge, M., Meggio, A., Pennelli, G., Piscioli, F., Giacomelli, L., de Pretis, G., & Graham, D. Y. (2007). Gastritis staging in clinical practice: The OLGA staging system. Gut, 56(5), 631–636.
- Coelho, M. C. F., et al. (2021). Helicobacter pylori chronic gastritis on patients with premalignant conditions: Olga and olgim evaluation and serum biomarkers performance. Arquivos de Gastroenterologia, 58(1), 39–47.
- Pimentel-Nunes, P., Libânio, D., Marcos-Pinto, R., et al. (2019). Management of epithelial precancerous conditions and lesions in the stomach (MAPS II): European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter and Microbiota Study Group (EHMSG), European Society of Pathology (ESP), and Sociedade Portuguesa de Endoscopia Digestiva (SPED) guideline update 2019. Endoscopy, 51(4)
Quer saber mais? Acompanhe esse outro post que preparamos para você.
Membro Titular da Sociedade Brasileira de Endoscopia Digestiva (SOBED);
Especialização em Endoscopia Digestiva na Universidade de São Paulo (USP);
Mestrado em Cirurgia na Universidade Federal de Pernambuco (UFPE);
Médico endoscopista da NeoGastro (PE);
Coordenador do Serviço de Endoscopia Digestiva do Hospital Otávio de Freitas (PE)

3 Comentários
Excelente artigo, Flávio. Parabéns! Gostaria de lançar um questionamento quanto às classificações OLGA /OLGIM: considerando que as lesões pré-cancerosas (atrofia e metaplasia) do antro são menos graves do que as do corpo (não há nem mesmo recomendação de seguimento endoscópico quando isoladas), qual a sua opinião para estas classificações darem mais importância às lesões de antro? Por exemplo: uma metaplasia / atrofia severa do antro combinada com nenhuma alteração do corpo é considerada Estágio III. Por outro lado, uma metaplasia / atrofia severa do corpo combinada com nenhuma alteração do antro é considerada Estágio II.
Excelentes comentários, como sempre precisos. O trabalho original descreve o local das biópsias em parede anterior e posterior e desta forma conseguiu mostrar nitidamente a relação da atrofia mais intensa (OLGA III/IV) com câncer sendo reproduzido em outras publicações. Estudos e guidelines mais recentes como o ESGE MAPSII atualizam a localização das biópsias para pequena e grande curvatura, citando ainda que o direcionamento das biópsias com aparelhos mais modernos de alta definição associados a cromoscopia são mais eficazes. Vale ressaltar que participaram desta publicação da ESGE outras três sociedades como a Sociedade Europeia de HP e microbiota, a Sociedade Europeia de Patologia e a Sociedade Portuguesa de Endoscopia Digestiva (SPED), validando a importância da localização das biópsias em pequena e grande curvatura.
Gosto do debate realmente, sempre é bom. Bem, eu faço sim as biópsias, em pequena e grande curvatura, uso a cromoscopia e “gasto” sim meu tempo procurando metaplasia e alterações mais significativas da mucosa. Acho que devemos manter nossa humildade de não julgar que a endoscopia isoladamente é suficiente para determinar a intensidade da atrofia e portanto do risco de degeneração maligna. Temos respaldo científico de que não são todos e sim os pacientes com escores mais elevados que requerem seguimento mais próximo. Fica mais fácil ser “surpreendido” com áreas de displasia e câncer se conseguirmos filtrar os pacientes que devem ficar mais próximos de nós e mantermos os olhos mais abertos durante estes exames. Podemos perder horas fazendo isso ao longo de nossa vida profissional mas um diagnóstico de câncer precoce dado pode salvar uma vida. Não foi por isso que escolhemos a medicina?
Grande abraço
Parabéns pelo artigo Flávio. Vou complementar com um comentário e deixar uma pergunta:
1. Locais das biópsias: OLGA original orienta realizar na parede anterior e posterior de corpo. Faz pouco sentido essa recomendação, visto que a progressão da linha de atrofia (linha F) ocorre pela pequena curvatura . Ou seja, poderia estar deixando de obter fragmentos de uma área atrófica de corpo. No guideline da ESGE MAPSII a orientação é realizar biópsias direcionadas (para quem tem bom aparelho e experiência) ou pelo menos bxs da pequena e grande curvatura de corpo.
2. Você fez uma pergunta provocativa: “É realmente necessário fazer essas biópsias? A avaliação endoscópica não é suficiente??” – qual sua opinião? As biópsias aleatórias poderiam nos surpreender com áreas de displasia ou câncer?