Introdução – Terminologia:
De acordo com a Classificação de Atlanta Revisada (1), as coleções fluídas peripancreáticas (CFPs) são agrupadas de acordo com:
- Tempo: 4 semanas
- Presença de componentes necróticos/sólidos
Esta nova classificação é importante pois o tratamento e o manejo variam de acordo com o tipo de coleção.
As CFPs são complicações frequentes da pancreatite aguda ou crônica. Estima-se que 5% a 15% dos episódios de pancreatite são complicados com o desenvolvimento de pseudocistos. Entretanto a maioria das CFPs irão resolver-se espontaneamente.
Indicações de Tratamento:
Considerar o tratamento para coleções crônicas (> 4 semanas) e sintomáticas.
Possíveis sintomas e complicações:
- Dor abdominal
- Obstrução gastrointestinal
- Compressão vascular
- Obstrução biliar
- Infecção
A drenagem das coleções deve ser feita após 4 semanas para permitir a maturação e o encapsulamento da lesão, com potencial redução das complicações quando a drenagem for realizada.
Tratamento endoscópico
Recomendado como terapia de primeira linha (Grau A de recomendação). (2) Ensaio-clínico controlado e randomizado comparando o tratamento endoscópico vs cirúrgico demonstrou:
- Sucesso técnico e taxa de complicações semelhantes;
- A terapia endoscópica foi associada com menor tempo de internação, menor custo e melhor qualidade de vida.
Estudo retrospectivo comparando a drenagem endoscópica vs percutânea favoreceu a endoscopia, pois esta última esteve associada com (3):
- Maior taxa de sucesso no tratamento;
- Menores taxas de re-intervenção;
- Menor tempo de internação.
Tipos de drenagem endoscópica:
- Drenagem transpapilar
- Drenagem transmural, que se divide em: convencional e ecoguiada.
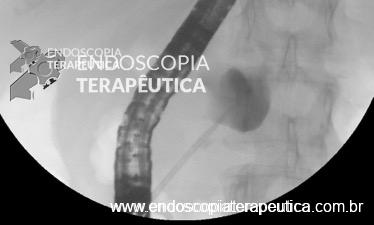
Drenagem Transpapilar:
Realizada através da CPRE com colocação de prótese plástica transpapilar idealmente até o interior da coleção.
Reservada para pequenas coleções (até 6 cm), localizadas na cabeça ou corpo proximal do pâncreas, e que se comunicam com o ducto pancreático principal. (2)
Drenagem Transmural Convencional:
Requer visualização endoscópica do abaulamento causado pela CFP no trato gastrointestinal. Entretanto esta apresentação com abaulamento é descrita em cerca de 42% a 48% dos casos, o que limita a eficácia e a segurança desta técnica em quase metade dos pacientes. (4)
Drenagem Transmural Ecoguiada:
Devido ao uso da ecoendoscopia, esta técnica apresenta a capacidade de identificar e evitar estruturas vasculares entre a coleção e o lúmen gástrico/enteral. Sendo fortemente indicada para os pacientes com coleções que não produzam abaulamento e nos pacientes com hipertensão portal. Apresenta taxa de sucesso de 94%, com taxa de complicação de 5% na drenagem de pseudocistos. (4) Atualmente, é a técnica estabelecida como a terapia de primeira linha na drenagem de pseudocistos e de necroses pancreáticas delimitadas (NPD), do inglês walled-off necrosis.
É tradicionalmente realizada com a colocação de pelo menos 2 próteses plásticas (menor chance de oclusão comparado com apenas 1 prótese) com formato em duplo pigtail (menor chance de migração comparado com as próteses retas). As próteses não devem ser retiradas antes da resolução do cisto (determinada pela revolução clínica e radiológica), e também não antes de pelo menos 2 meses (Grau B de recomendação). (2)
Abaixo vídeo demonstrando a técnica (gentilmente cedido por Dr Madhu Sanaka):
Mais recentemente próteses metálicas auto-expansíveis cobertas (PMAEc) passaram a ser utilizadas para durante a drenagem ecoguiada. As vantagens da utilização da PMAEc são:
- Necessidade de apenas um único stent, portanto, simplificando e encurtando o procedimento;
- O maior diâmetro da prótese, possibilitando uma drenagem mais rápida, com menor risco de oclusão;
- E o potencial para entrar na colecção repetidamente com um gastroscópio para a realização de necrosectomia.
Recentes publicações demonstraram melhores resultados para a drenagem de pseudocistos e NPDs com o uso de PMAEc, quando comparadas com próteses plásticas, com benefícios em relação (6-8):
- Tempo de procedimento mais curto;
- Maior taxa de resolução;
- Menor taxa de complicações.
No entanto, uma importante preocupação com o uso de PMAEc é o risco de migração, levando alguns endoscopistas a colocarem uma prótese plástica de duplo pigtail por dentro da prótese metálica para sua ancoragem.
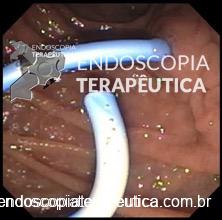
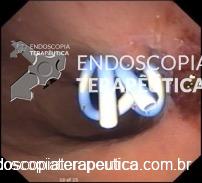
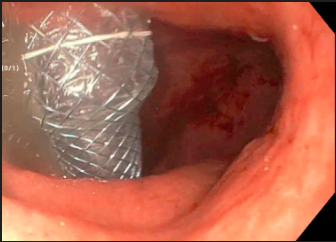
Para diminuir o risco de migração das PMAEc, novas próteses metálicas foram concebidas com bordas que possibilitam a aposição de lumens (figuras abaixo). As vantagens desses próteses são:
- Possuem largas falanges de ancoragem e evitam a necessidade de colocar uma prótese plástica de ancoragem;
- Apresentam largo diâmetro interno (10 ou 15 mm), que possibilita a realização da necrosectomia endoscópica através da prótese;
- Presença de cautério na ponta de sua agulha de punção que possibilita a liberação da prótese sem a necessidade de uso de outros materiais.
Na literatura existe apenas um recente estudo retrospectivo comparando as PMAEc com as próteses metálicas para aposição de lumens (PMAL), realizado por Siddiqui et al (9). Esta publicação, com pacientes submetidos à drenagem endoscópica da NPDs, demonstrou:
- Não houve diferença quanto às taxas de sucesso técnico e clínico, e sucesso a longo prazo (necessidade de intervenção após 6 meses da remoção da prótese);
- Menor número necessário de procedimentos com o uso PMAL;
- Entretanto, houve uma maior taxa de complicações precoces com o uso das PMAL.
Os autores justificaram que as complicações precoces, com ocorrência principalmente de perfurações, foram resultados da falha na liberação da prótese pelo operador, e não devido ao design da prótese. Essas complicações ocorreram principalmente no início do estudo e estiveram associadas com a curva de aprendizado do endoscopista. Com relação às complicações tardias, houve menor taxa de migração com as PMAL, como esperado pelo autores.
Abaixo vídeo demonstrando o uso da PMAL (gentilmente cedido por Dr Prabhleen Chahal):
Drenagem da necrose pancreática delimitada (NPD):
- Dar preferência para o uso de próteses metálicas, pela necessidade da realização de necrosectomia;
- Considerar a associação de dreno nasocístico, uma vez que publicação demonstrou que pode produzir menor taxa de oclusão das próteses e maior taxa de resolução. (10)
- Considerar a técnica de múltiplos acessos transmurais, que pode estar associada com maior taxa de sucesso clínico. (11)
Link para caso de drenagem de CPF com necrosectomia: aqui!
Qual a necessidade da CPRE na drenagem das CFP?
Estudo retrospectivo multicêntrico (12), com 375 pacientes (54% com NPD) submetidos a drenagem endoscópica, comparou a drenagem transmural ecoguida isolada versus drenagem combinada (transmural ecoguiada + transpapilar por CPRE), e observou que não houve diferença na taxa de sucesso clínico entre ambas a terapias. Assim, a CPRE tem sido reservada para casos selecionados, por exemplo para pacientes com suspeita de fístula pancreática ou coleções recorrentes. A CPRE em associação com a drenagem transmural tem por objetivo a colocação de uma prótese “em ponte” para oclusão do rompimento no ducto pancreático.
Referências:
- Banks PA, et al. Gut 2013, 62:102
- Dumonceau J-M, et al. Endoscopy 2012, 44: 784
- Keane MG, et al. Surg Endosc 2016.
- Antillon MR, et al. Gastrointest Endosc 2006; 63: 797
- Sadik R, et al. Word J Gastroenterol 2012; 17: 499
- Sharaiha RZ, et al. Gastrointest Endosc. 2015;1
- Mukai S, et al. Endoscopy 2015;47
- Lee BU, et al. Endoscopy. 2014;1078.
- Siddiqui AA, et al. Gastrointest Endosc. 2016;
- Siddiqui AA, et al. Gastrointest Endosc 2013.
- Varadalajulu S, et al. Gastrointest Endosc 2011.
- Yang D, et al. Gastrointest Endosc. 2016;83(4):720
Advanced Endoscopy Fellowship na Cleveland Clinic, Ohio, EUA.
Doutorado em Gastroenterologia pela FMUSP.
Mestrado na Escola Paulista de Medicina – UNIFESP/EPM.
Membro titular da SOBED e FBG.
-
Matheus Francohttps://endoscopiaterapeutica.net/pt/author/matheus/
-
Matheus Francohttps://endoscopiaterapeutica.net/pt/author/matheus/
-
Matheus Francohttps://endoscopiaterapeutica.net/pt/author/matheus/
-
Matheus Francohttps://endoscopiaterapeutica.net/pt/author/matheus/





2 Comentários
Bruno obrigado pelo comentário!
1. A via transpapilar tem caído em desuso. No texto faço referência às recomendações dadas pelo guideline da ESGE que foi publicado em 2012. De lá para hoje, bastante coisa já mudou sobre esse tema. A drenagem transmural, de preferência com ecoendoscopia, é o método de eleição. A utilização de ecoendoscopia tem crescido bastante, e cada vez mais nos deparamos com novos equipamentos para auxílio na terapêutica ecoendoscópica. Se nos basearmos nas recomendações da ESGE de 2012, acredito que iremos realizar a drenagem transpapilar para pouquíssimos pacientes. Pois esse técnica foi recomendada para pseudocistos pequenos apenas (5 cm), e os pseudocistos que produzem sintomas geralmente são maiores que 6 cm. Atualmente a indicação recai mais na presença de sintomas, e não mais no tamanho do cisto. Outra desvantagem da técnica, como você bem levantou, é que apesar de a TC poder mostrar comunicação do pseudocisto com o DP a melhor maneira para descobrir a comunicação é com a pancreatografia durante a CPRE.
2. Apesar de haver sim esse risco teórico as publicações com essa técnica (década de 90 e início dos anos 2000) mostraram uma taxa de sucesso relativamente boa. Mas, novamente, a técnica transpapilar isoladamente com colocação de prótese no interior da coleção está em desuso. E atualmente a CPRE quando realizada em combinação com a drenagem transmural objetiva a colocação de uma prótese “em ponte” através do defeito do ducto pancreático.
3. Essa é uma ótima pergunta também Bruno!
A melhor resposta acho que é: utilize a prótese que você tem disponível e que também seja condizente com o cenário que você trabalha.
Num ambiente ideal, eu optaria sim por uma prótese metálica mesmo para o pseudocisto simples, por tornar o procedimento mais rápido, simples, e ter produzido evidência com maior taxa de resolução e menor taxa de complicações, quando comparado com o uso de próteses plásticas pig-tail. Esse foi um trabalho retrospectivo publicado em 2015 na GIE por Sharaiha et al (referência 6 do texto), com 230 pacientes com pseudocistos simples que foram drenados por endoscopia.
Abraço!
Parabéns pela revisão extremamente didática Matheus!
Algumas dúvidas:
1. Visto que a via de escolha para drenagem das CFP seria a via transmural, quando você decide pela via transpapilar? A única maneira de saber se existe uma comunicação persistente entre o DPP e a coleção seria fazendo uma pancreatografia, que obviamente não fazemos em todos os casos. Então, quando fazer?
2. Ainda sobre a via transpapilar, se a prótese deve ser inserida até o interior da coleção, não poderia perpetuar o defeito ductal?
3. Para tratamento do pseudocisto simples (sem necrose), tendo a opção de stent metálico e próteses plásticas pig-tail, qual você utilizaria?
Abs