Paciente 66 anos, sexo feminino, sem queixas, veio para exame de endoscopia digestiva alta (EDA) para avaliação pré-operatória (gastroplastia redutora).
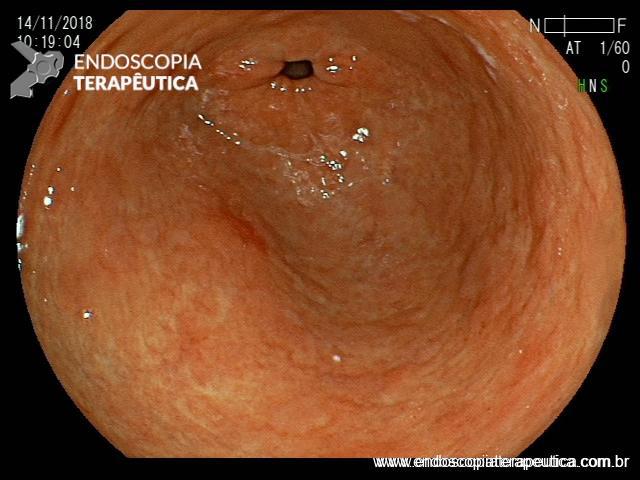
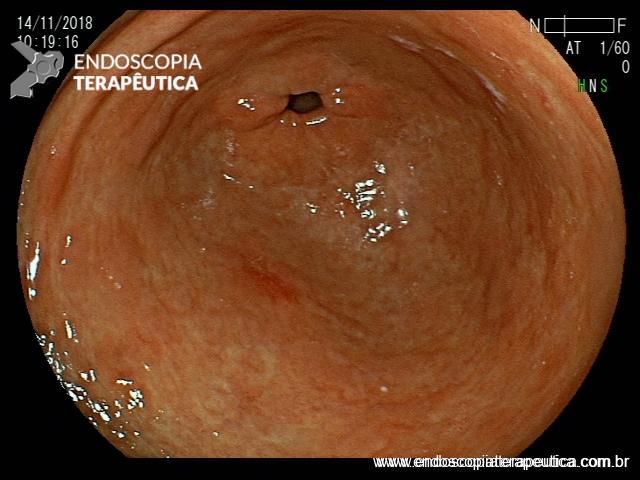
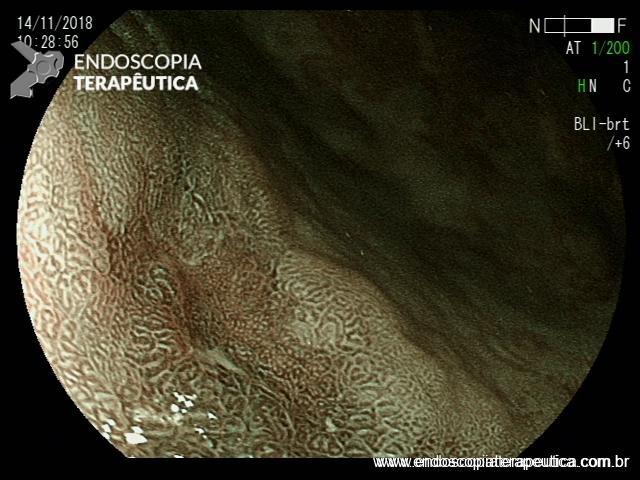
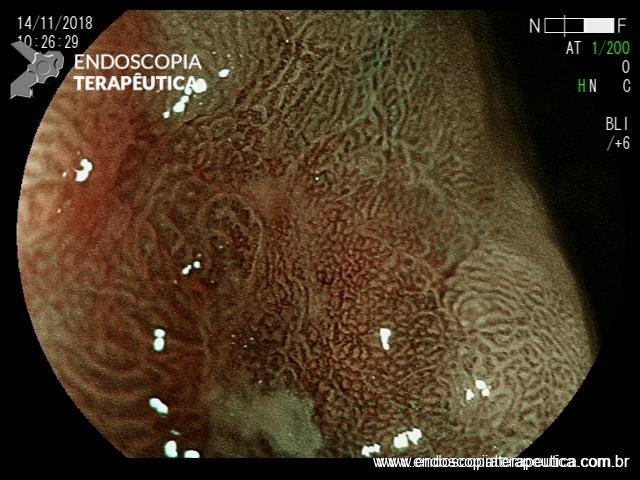
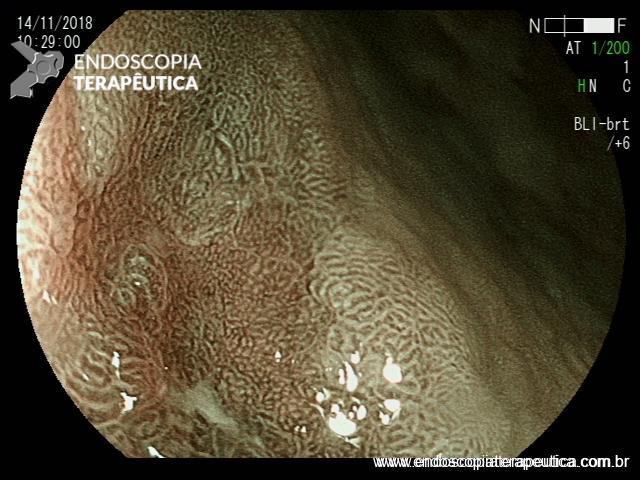
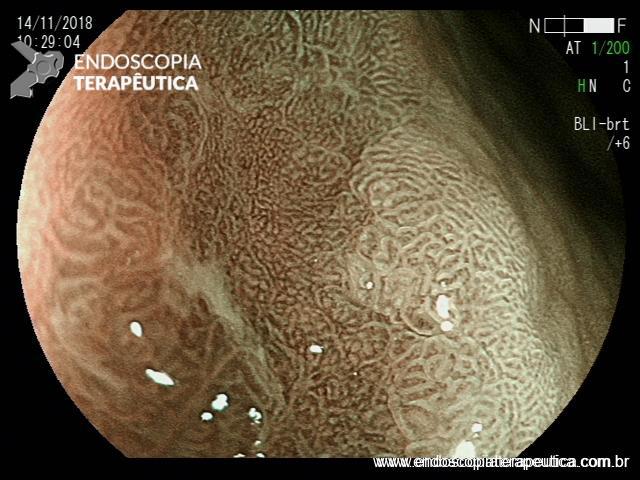
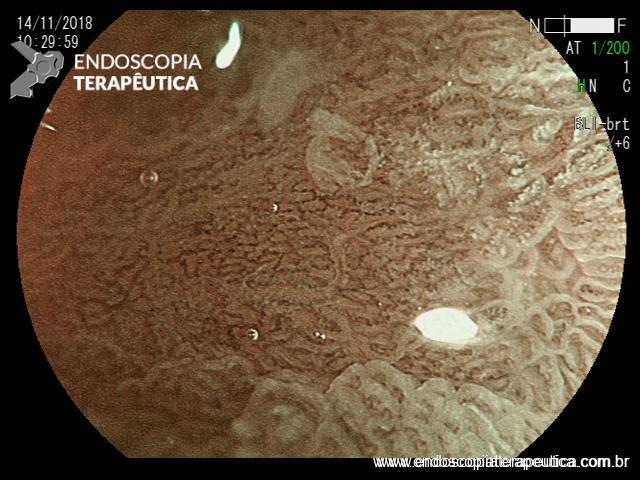
Após lavagem abundante da câmara gástrica com água e simeticona, identificada gastrite atrófica com metaplasias intestinais em antro, e lesão deprimida suspeita (0-IIc / Classificação de Paris), medindo cerca de 1,5 cm, localizada na grande curvatura para parede anterior de antro distal, fotos a seguir:
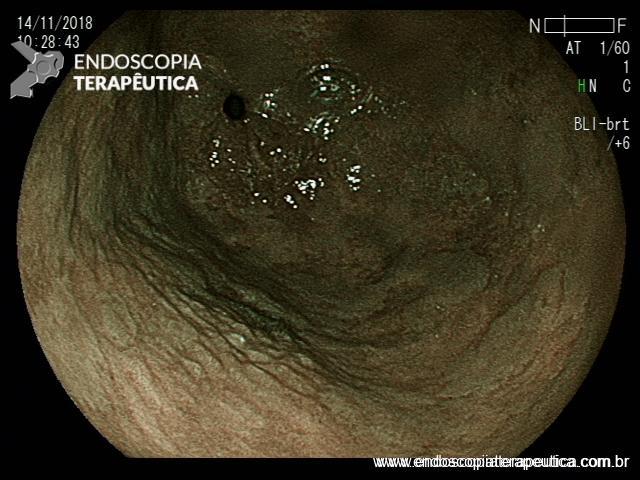
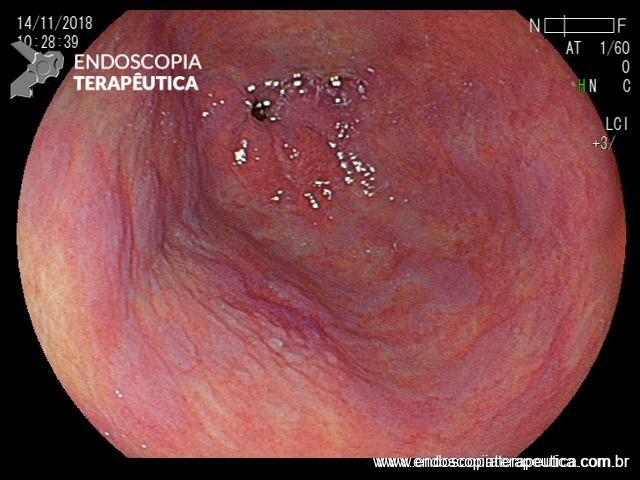
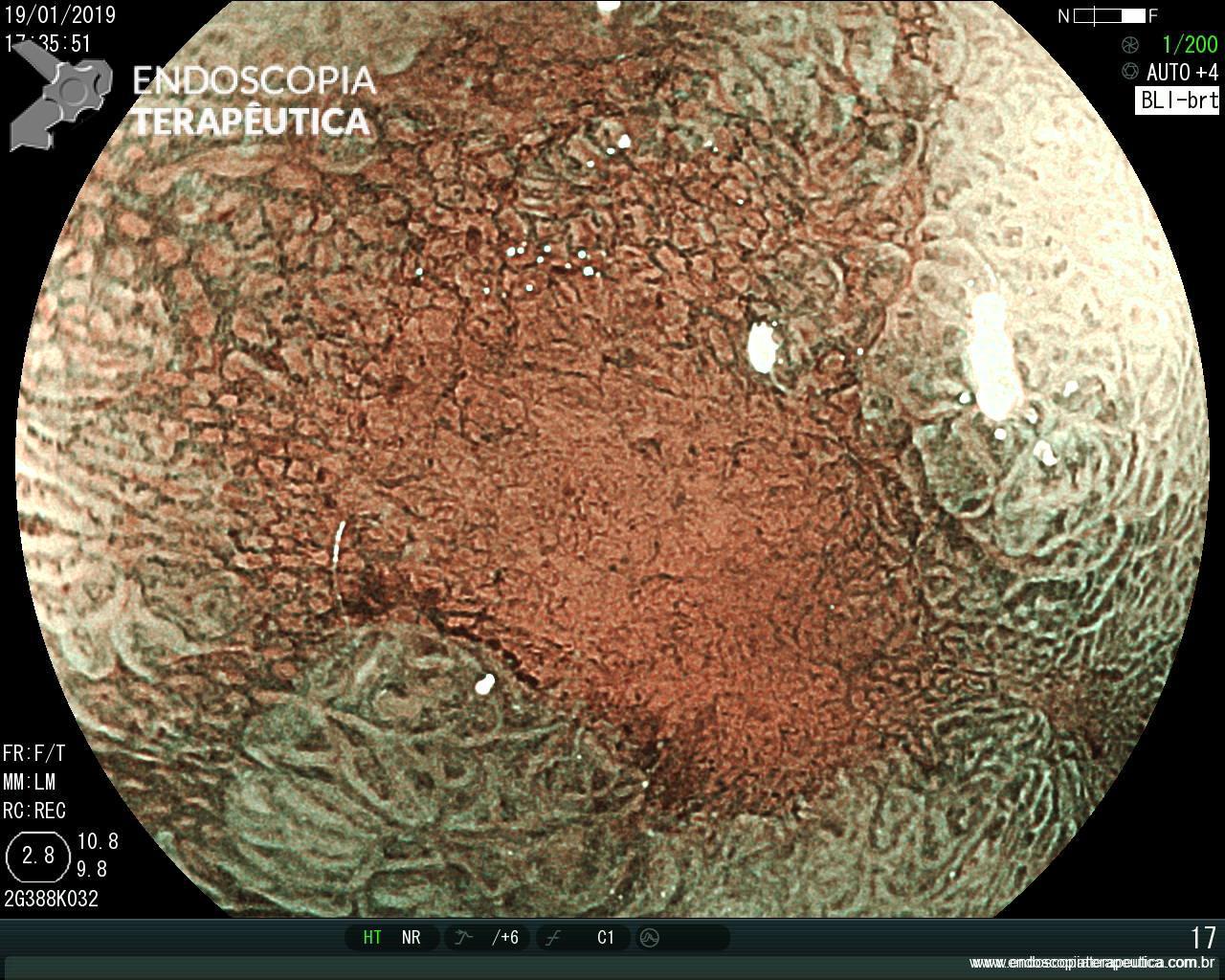
Após identificação da lesão com luz branca e com uso da cromoscopia óptica, realizada avaliação com uso da magnificação, sendo possível observar com mais detalhes a linha demarcatória, e a irregularidade das criptas e da vascularização no leito da lesão:
A biópsia demonstrou adenocarcinoma bem diferenciado, intramucoso. A paciente foi então encaminhada para realização de estadiamento com ecoendoscopia, que evidenciou que lesão não apresentava sinais de invasão da submucosa, e não se observaram linfonodomegalias (eusT1aN0Mx).
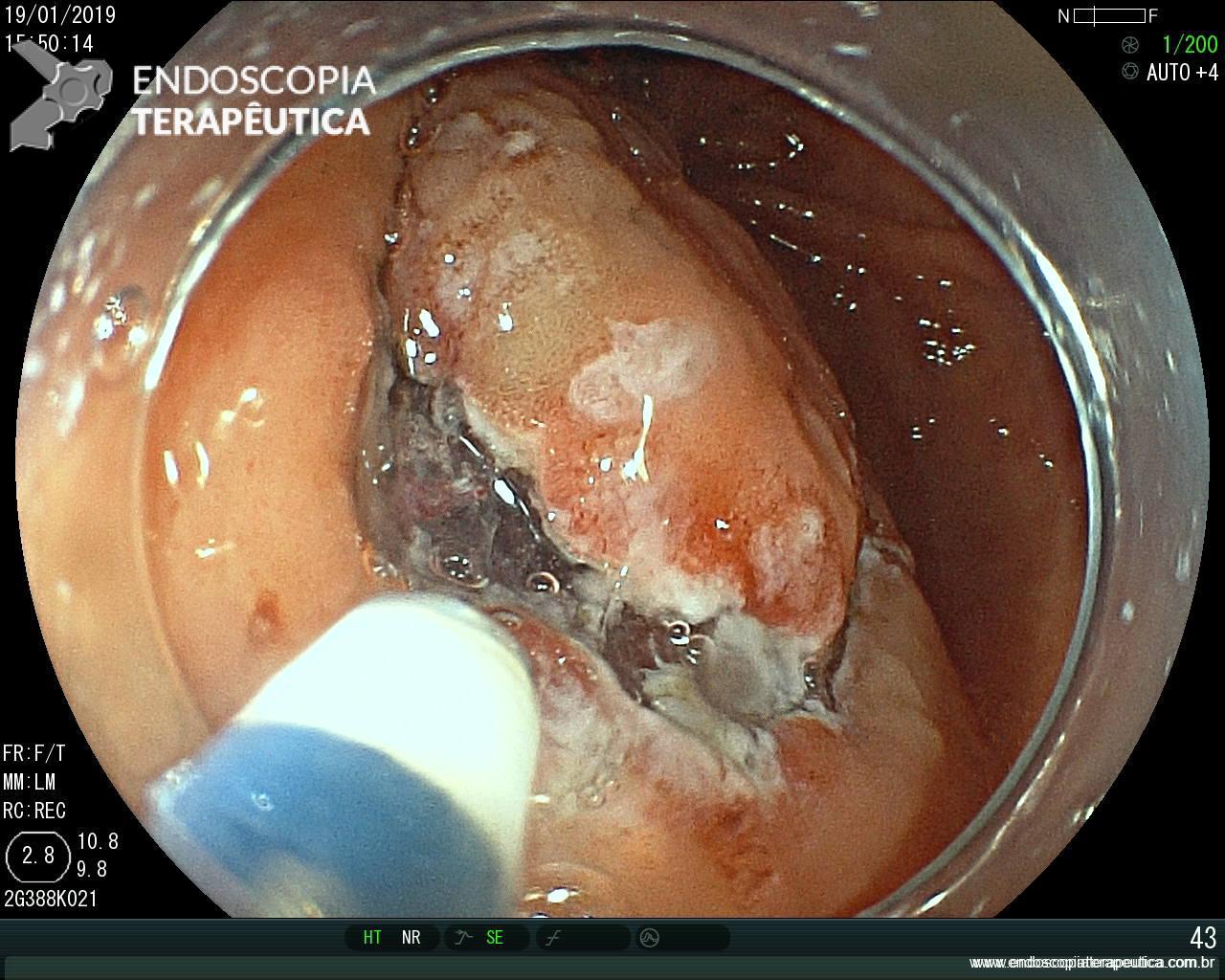
Paciente foi então encaminhada para realização de ressecção da lesão gástrica pela técnica de dissecção endoscópica da submucosa (ESD) com o Dr Nelson Miyajima (H. Nipo-Brasileiro).
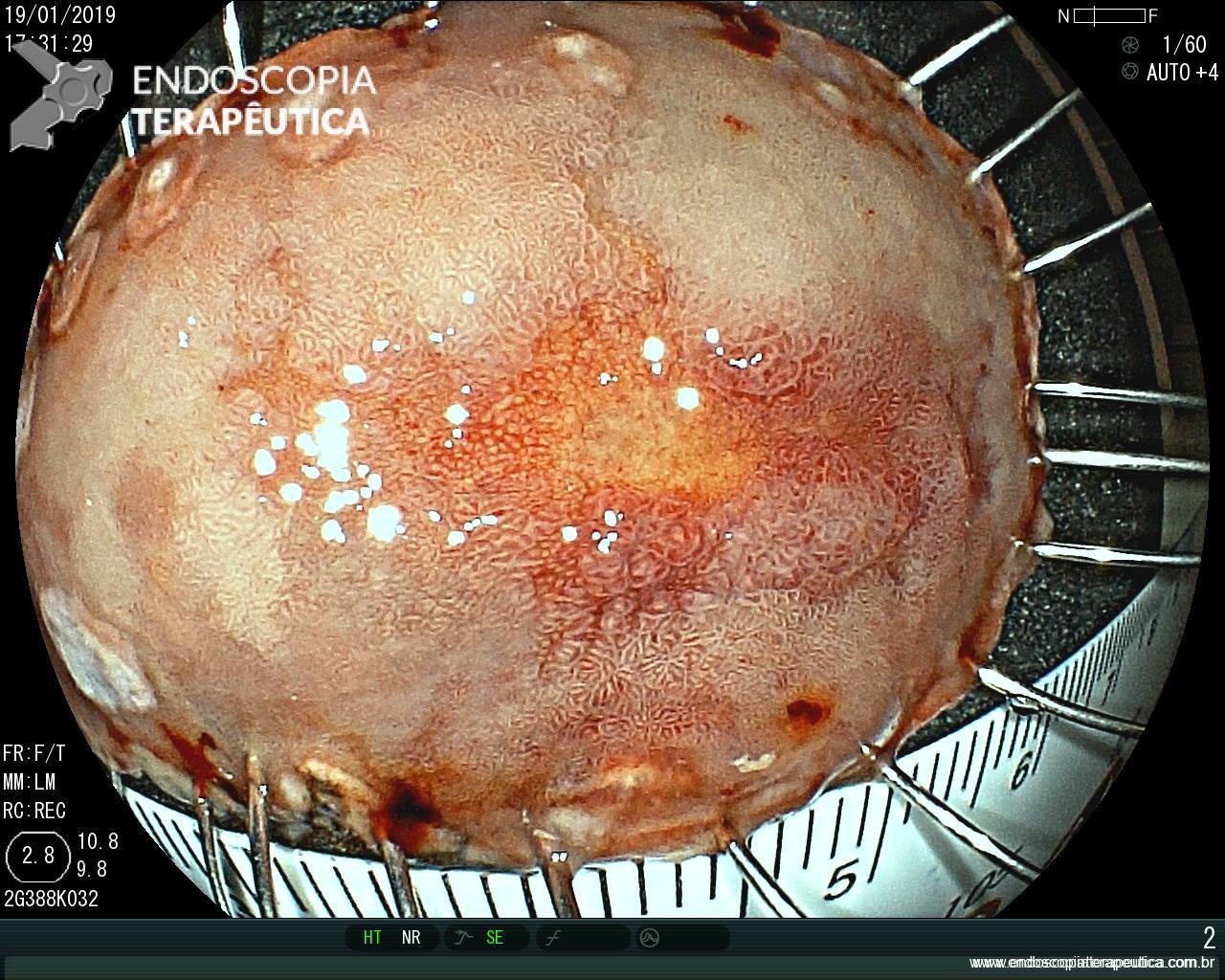
Procedimento ocorreu sem intercorrências. E o AP evidenciou adenocarcinoma bem diferenciado, restrito a mucosa, ausência de invasão linfovascular, e margens livres (estadiamento pTis).
Veja mais sobre: processo de limpeza e desinfecção de endoscópios
Advanced Endoscopy Fellowship na Cleveland Clinic, Ohio, EUA.
Doutorado em Gastroenterologia pela FMUSP.
Mestrado na Escola Paulista de Medicina – UNIFESP/EPM.
Membro titular da SOBED e FBG.